当您委托的业务完成后,您可以向服务顾问提出开具服务发票申请,我们将尽快给您出具相应的服务发票;第三方服务内容,由第三方为您出具相应的服务发票。
咨询电话:



在医疗器械领域,欧盟委员会制定了三个欧盟指令,以替代原来各成员的认可体系,使有关这类产品投放市场的规定协调一致。分别为:
医疗器械指令MDD
93/42/EEC,适用范围很广,包括除有源植入性和体外诊断器械之外的几乎所有的医疗器械。
体外诊断指令IVDD
98/79/EC,适用于血细胞计数器,妊娠检测装置等活体外诊断用医疗器械。
有源植入性医疗器械指令AIMDD
90/385/EEC,适用于心脏起搏器,可植入的胰岛素泵等有源植入性医疗器械。
MDR简介
新法规 MDR (EU) 2017/745,2020年5月份强制实行MDR新法规。MDR是法规,MDD是指令。因为是升级,从指令升级为法规,所以欧盟成员国都会对认证过程和结果进行更加严格的控制。
MDR欧代和MDD欧代的区别是什么?
欧盟授权代表(AR)是指在欧盟境内的任何自然人或法人,其收到并接受位于欧盟以外的制造商的书面授权,代表该制造商按照本法规对制造商所规定的义务要求所进行的一切行动。AR是您与欧洲当局的联系的桥梁,他们必须是在欧洲有实体存在。AR保存制造商的技术文件,供主管部门检查。AR的名称和地址必须器械随附的信息上,例如(包装)标签和使用说明。如果发生事故,AR将协助并协调向主管当局报告事件。
MDR下的欧代相比于MDD下的欧代,要求更加严格,责任也更大。除了负有以上义务之外,还会与制造商一样为缺陷器械承担连带的法律责任。另外,授权代表应至少有一名可永久且持续听其调遣的负责法规符合性的人员,其在欧盟境内的医疗器械监管要求方面拥有必要的专业知识。必要的专业知识应表现为以下任一一种资格:
(a) 在完成有关成员国确认为同等学历的法律、医学、药学、工程或其他相关科学学科大学学历或学习课程后颁发的文凭、证书或其他正式资格证书,以及在体外医疗器械相关法规事务或质量管理体系方面具有至少一年专业经验;
(b) 在法规事务或与医疗器械有关的质量管理体系方面有四年的专业经验。
MDD指令根据不同的要求共分为6个等级,供认证机构评估:
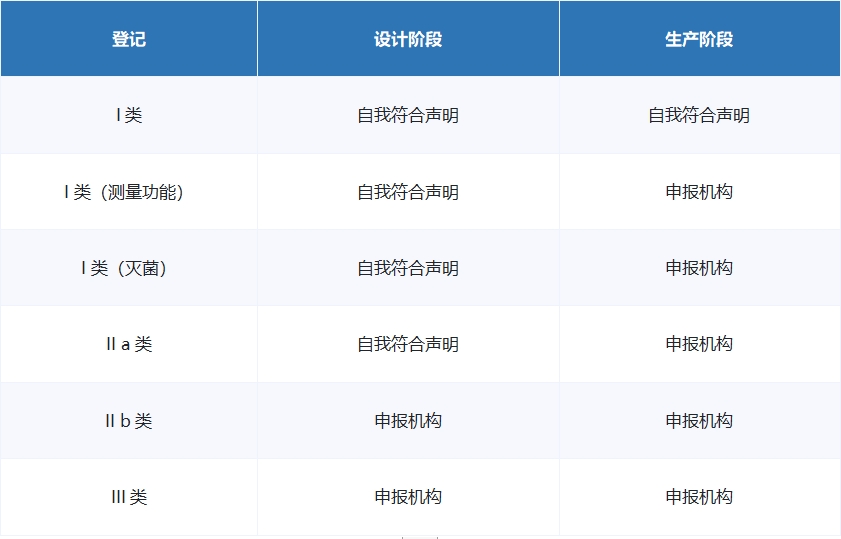
医疗器械认证所需技术资料
认证机构的统一评估包括根据指令规定的基本要求评审技术文件、根据标准EN 46001 或 EN/ISO 13485评审质量体系。医疗设备CE认证技术档案所需内容:
- 生产商/或欧洲代表名址;
- 产品及型号描述;
- EC符合声明书;
- 风险评估;
- 基本安全点检表;
- 适用之调合标准/或其他标准;
- 市场反馈及抱怨分析;
- 使用说明及标签;
- 授权代表;
- 线路、图表(适用的话);
- 计算书、测试报告或其它证明材料;
- 检验过程及过程描述;
- 灭菌或其它特殊过程(适用的话);
- 灭菌类产品的包装材料及方法;
- 质量体系、质量手册;
签发CE认证的机构:
欧盟公告号NB机构(NotifyBody)签发
国内实验室签发
http://ec.europa.eu/growth/single-market/european-standards/harmonised-standards
医用非灭菌口罩如何办理CE自我声明?
CE自我声明由产品制造商或其在欧盟的授权代表(以下简称“欧代”)签署“符合性声明”(Self Declaration of Conformity),并准备相关技术文件。
以医用非灭菌口罩为例:自我声明需要企业建立质量管理体系(非必须)+技术文档 (包括产品信息,组成材料,风险管理,基本要求,适应标准,临床评估,标签说明书等等),提供产品测试报告(如口罩本身的生物学、性能等测试报告,需符合EN14683)、欧代授权协议、CE符合性声明等材料,由欧代经欧盟成员国注册后,企业即可完成CE自我声明,并自行加贴(印制)CE标志。CE自我声明无CE证书。监管过程中可核实上述材料,进行综合判定。
国外/国内某机构发的“CE Documentation Review”(CE 文件审核证明),是否是认证证书?
国外/国内机构给国内企业颁发的文件审核证明不应界定为认证证书。发现该类证明后,地方市场监管部门应调查核实企业获取证明的过程,重点核实相关机构(咨询机构、代理机构、国内发证机构)在给企业办证过程中是否存在有虚构事实或隐瞒真相,使企业陷入错误认识的情形,认为办理“CE Documentation Review”就符合了欧盟要求,即可加贴CE标志。
 什么时候可以拿到服务发票?
什么时候可以拿到服务发票? 
当您委托的业务完成后,您可以向服务顾问提出开具服务发票申请,我们将尽快给您出具相应的服务发票;第三方服务内容,由第三方为您出具相应的服务发票。
 支付流程
支付流程 
签订协议、材料准备、特约快递、收取票据、专属客服、商务对接、资质申报、完成办理、提供发票